
7 Ejemplos de fusión
Algunos ejemplos de puntos de fusión son los siguientes: Punto de fusión del agua sólida (hielo) (H 2 O): 0 ºC. Punto de fusión del cobre (Cu): 1085 ºC. Punto de fusión del aluminio (Al): 660 ºC. Punto de fusión del oro (Au): 1064 ºC. Punto de fusión de la plata (Ag): 962 ºC.

En el ciclo del carbono, ¿qué sucede con el carbono que se libera durante la combustión? 2023
Se define punto de fusión como la temperatura a la cual un elemento químico cambia de la fase sólida a la líquida, a la presión de una atmósfera. En el Sistema Internacional de Unidades (SI) se mide en K (Kelvin). Para convertir a ºC (grados Celsius) se utiliza la siguiente expresión: Temperatura (K) = Temperatura (ºC) + 273.15.

El ciclo del carbono ciclo biogeoquímico Química Wikisabio
Punto de fusión del agua sólida (hielo) (H 2 O): 0 ºC. Punto de fusión del cobre (Cu): 1085 ºC. Punto de fusión del aluminio (Al): 660 ºC. Punto de fusión del oro (Au): 1064 ºC. Punto de fusión de la plata (Ag): 962 ºC. Punto de fusión del acero: alrededor de 1375 ºC (dependiendo de su aleación) Punto de fusión del carbono (C.

Estados de la Materia Puntos de Fusión y Ebullición YouTube
Punto de fusión. 3948,15 K | 3675 °C | 6647 °F. Punto de ebullición. 4300,15 K | 4027 °C | 7280,6 °F. Entalpía de fusión. 105 kJ/mol.. El principal uso industrial del carbono es como un componente de hidrocarburos, especialmente los combustibles fósiles.

Punto De Fusion Del Carbono chefli
El número atómico del carbono es 6. El símbolo químico del carbono es C. El punto de fusión del carbono es de diamante: 3823 KGrafito: 3800 K grados Kelvin o de -272,15 grados celsius o grados centígrados. El punto de ebullición del carbono es de grafito: 5100 K grados Kelvin o de -272,15 grados celsius o grados centígrados. Usos del.
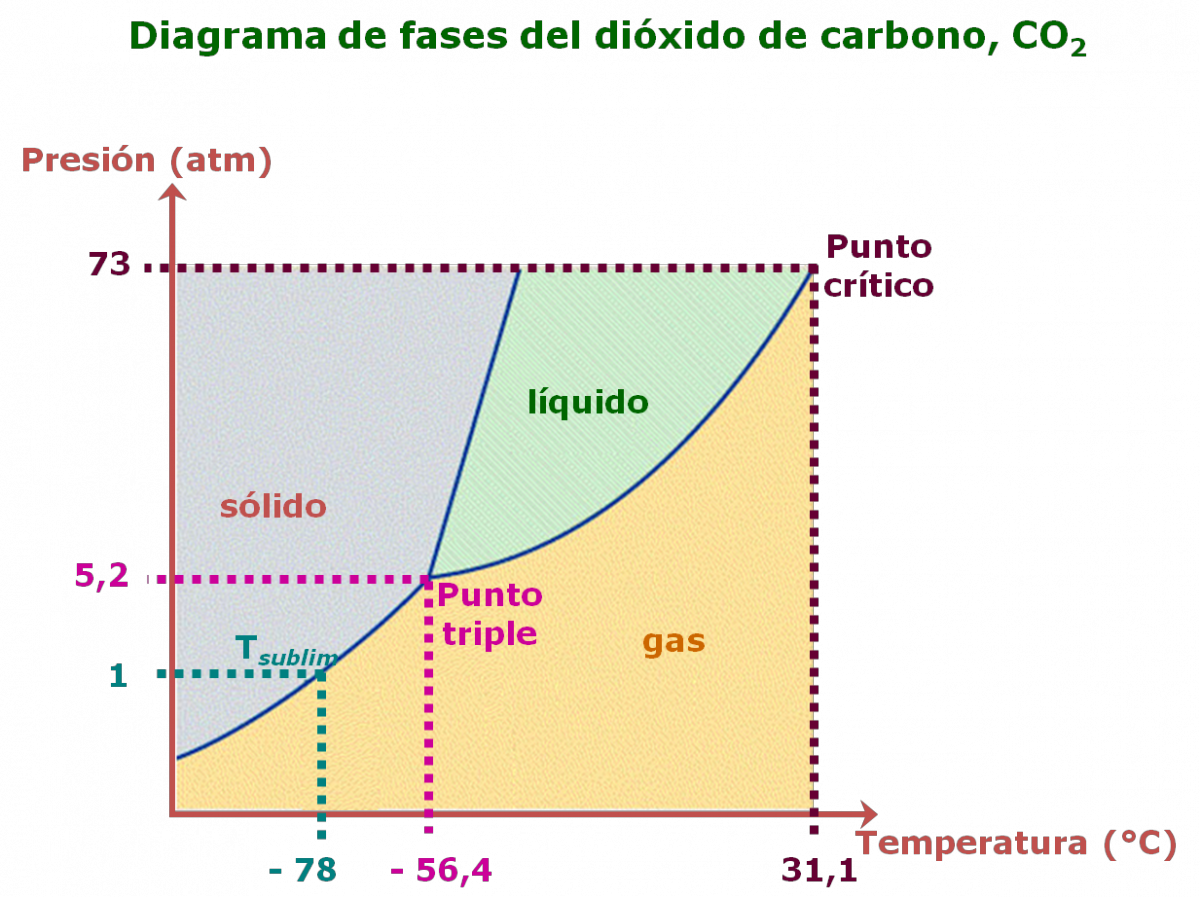
5.6. Cambios de estado Diagramas de calentamiento Diagramas de fase Química general
24. Punto de fusión. Es la temperatura a la que el elemento cambia de la fase sólida a la líquida, a la presión de 1 atm. En el Sistema Internacional se mide en K (Kelvin). En las sustancias puras, el proceso de fusión ocurre a una temperatura constante. La variación periódica de esta propiedad puede apreciarse con mucha facilidad en la.

Quimica Organica Alcanos
De Wikipedia, la enciclopedia libreEl carbono (del latín, carbo, 'carbón') es un elemento químico con símbolo C, número atómico 6 y masa atómica 12,01.Es un no metal y tetravalente, disponiendo de cuatro electrones para formar enlaces químicos covalentes. Tres isótopos del carbono se producen de forma natural, los estables 12 C y 13 C y el isótopo radiactivo 14 C, que decae con una.

Ciclo del Carbono y oxígeno. ECOLOGÍA Y MEDIOAMBIENTE
Ciclo de Fusión del Carbono. En las estrellas con temperaturas centrales superiores a 15 millones de grados Kelvin, la fusión de carbono se cree que asume el papel dominante en lugar de la fusión de hidrógeno.El objeto principal del ciclo del carbono consiste en la adición de protones, pero después el núcleo de carbono-12 se funde con otro protón para formar nitrógeno-13, luego uno de.

Punto de fusión y ebullición (1)
Primer potencial de ionización (ev): 11,34. Densidad a 20 °C: 2,267 g/cm³ (gr), 3,513 g/cm 3 (di) Entre las propiedades físicas del carbono, destacan su capacidad de formar una gran cantidad de compuestos, su solidez en formas como el diamante y su capacidad conductiva en estructuras como el grafito. Estas propiedades lo convierten en un.
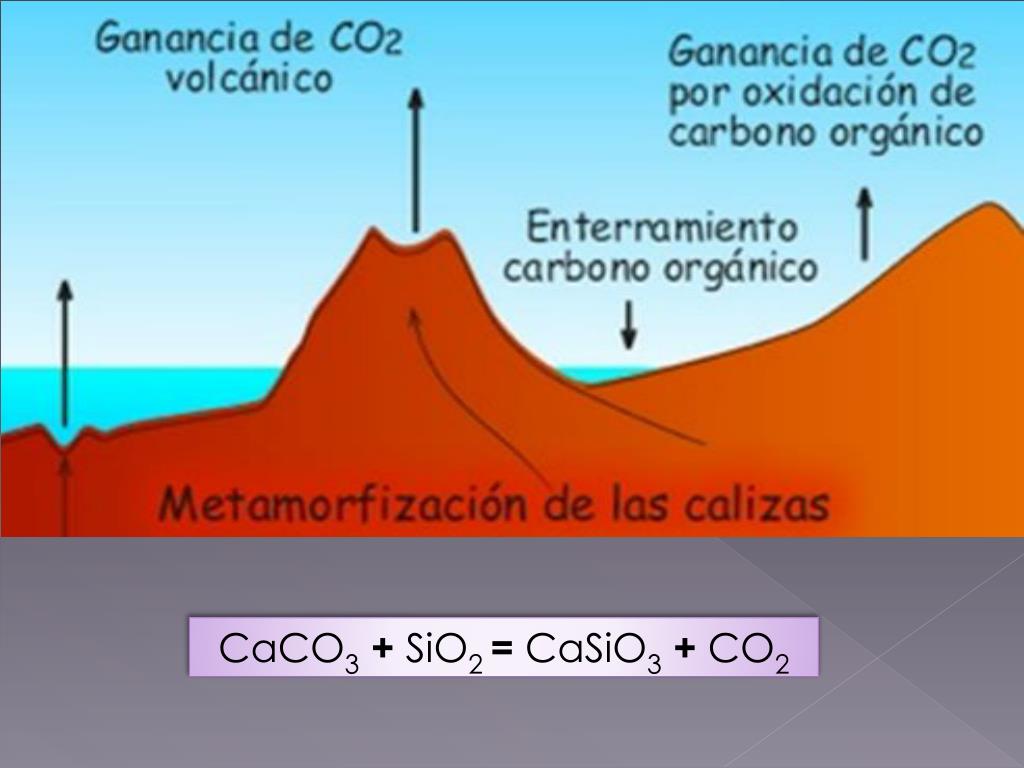
PPT CICLO DEL CARBONO PowerPoint Presentation, free download ID3869999
El carbono (del latín, carbo, 'carbón') es un elemento químico con símbolo C, número atómico 6 y masa atómica 12,01.Es un no metal y tetravalente, disponiendo de 4 electrones y 6 protones para formar enlaces químicos covalentes.Tres isótopos del carbono se producen de forma natural, los estables 12 C y 13 C y el isótopo radiactivo 14 C, que decae con una vida media de unos 5730 años.
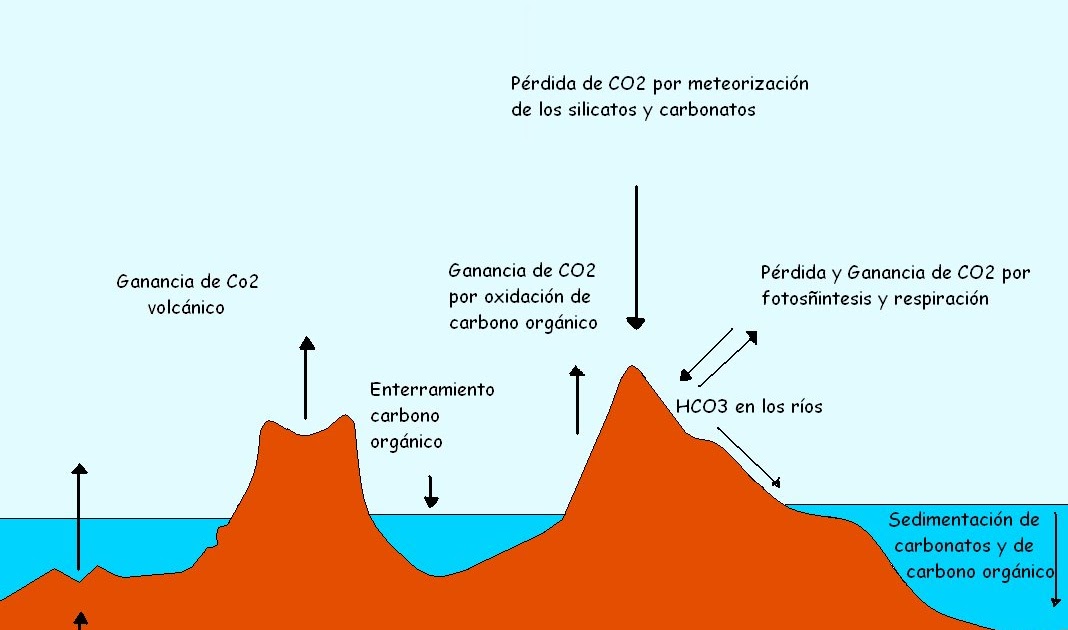
CICLOS DE LA NATURALEZA Diagrama Ciclo del Carbono
El punto de fusión del grafito es de 3500ºC (6332ºF) y el de ebullición extrapolado es de 4830ºC (8726ºF). El carbono elemental es una sustancia inerte, insoluble en agua, ácidos y bases diluidos, así como disolventes orgánicos. A temperaturas elevadas se combina con el oxígeno para formar monóxido o dióxido de carbono.

Ciencias 28 Saber 11 ICFES Temperaturas de Fusión y Ebullición de Materiales YouTube
Obsérvese también que el punto de ebullición para el tolueno es de 111 o C, muy por encima del punto de ebullición del benceno (80 o C). El factor clave para la tendencia del punto de ebullición en este caso es el tamaño (el tolueno tiene un carbono más), mientras que para la tendencia del punto de fusión, la forma juega un papel mucho.

🌡 Puntos de Fusión y Ebullición 🔥 ¿Qué son? EJEMPLOS [Fácil y Rápido] FÍSICA QUÍMICA YouTube
El carbono se une al oxígeno para formar el ion carbonato CO 32- y contribuye a una importante clase de minerales, los carbonatos. El carbono tiene una densidad de 2,26 en la forma de grafito, y 3,51 en la forma de diamante. Las formas cristalinas del diamante imperfectamente formadas se llaman bort o diamante negro.

Punto de fusión y ebullición (1) [PPTX Powerpoint]
Punto de fusión. Se conoce como punto de fusión a la temperatura en la cual una materia que se halla en estado sólido pasa a estado líquido. Para que se produzca el cambio de estado, deben de cumplirse ciertos requisitos como por ejemplo que la temperatura sea siempre constante. El punto de fusión es una propiedad física e intensiva que.
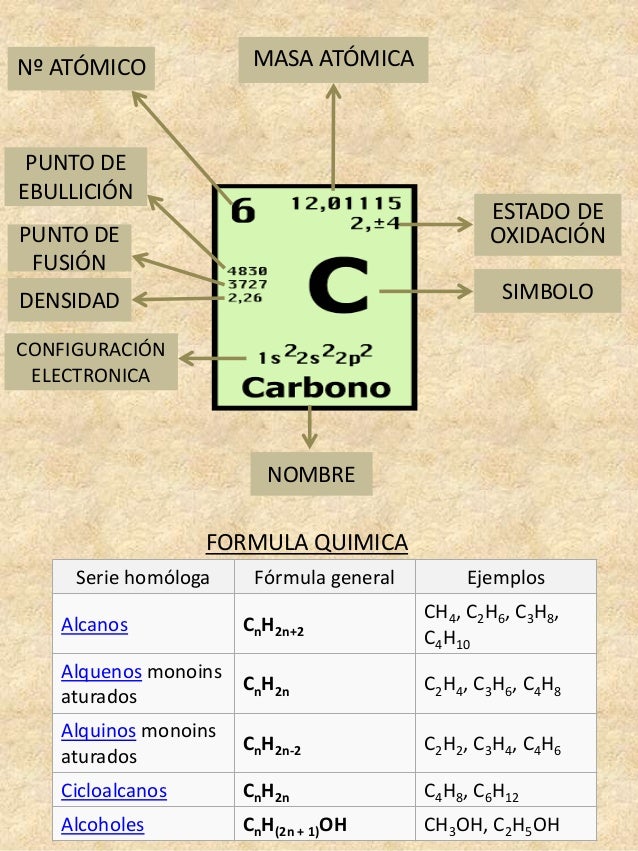
El Carbono (C)
El punto de fusión (Mp) es un análisis rápido y fácil que puede usarse para identificar cualitativamente muestras relativamente puras (aproximadamente < 10% de impurezas). También es posible utilizar este análisis para determinar cuantitativamente la pureza. El análisis del punto de fusión, como su nombre indica, caracteriza el punto de.

PPT CICLO DEL CARBONO PowerPoint Presentation, free download ID3869999
alotrópicas (con diferentes propiedades): diamante y grafito. Tiene alto punto de ebullición y fusión. PROPIEDADES QUÍMICAS: -Covalencia: El átomo de carbono se combina con átomos de otros elementos como el C, H, O y N mediante la compartición de electrones, es decir, formando enlaces covalentes. Ej. Metano H H H H C
- Globo Aerostático Que Puede Ser Manejado
- Direccion De Policia Federal En Iztapalapa
- Boletos Para Leo Dan Teatro Morelos
- Películas De John Travolta En Español
- Autobus Aeropuerto Cdmx A Queretaro
- 2002 Nissan Xterra V6 Supercharged
- Pinzas De Presion Para Pc
- Por Tres Puntos Cualesquiera Solo Puede Trazar Un Plano
- Hall Oates Philadelphia Freedom
- Donde Se Invento La Primera Locomotora De Vapor