
Modelo Atómico de Schrödinger » Modelos Atomicos
Se le conoce como "Modelo Cuántico-Ondulatorio" y fue propuesto por Erwin Schrödinger, en 1926, a partir de los estudios de De Broglie, Bohr y Sommerfeld. Su modelo concibe los electrones como ondulaciones de la materia, es decir, describe el comportamiento ondulatorio del electrón. Schrödinger sugirió que el movimiento de los.
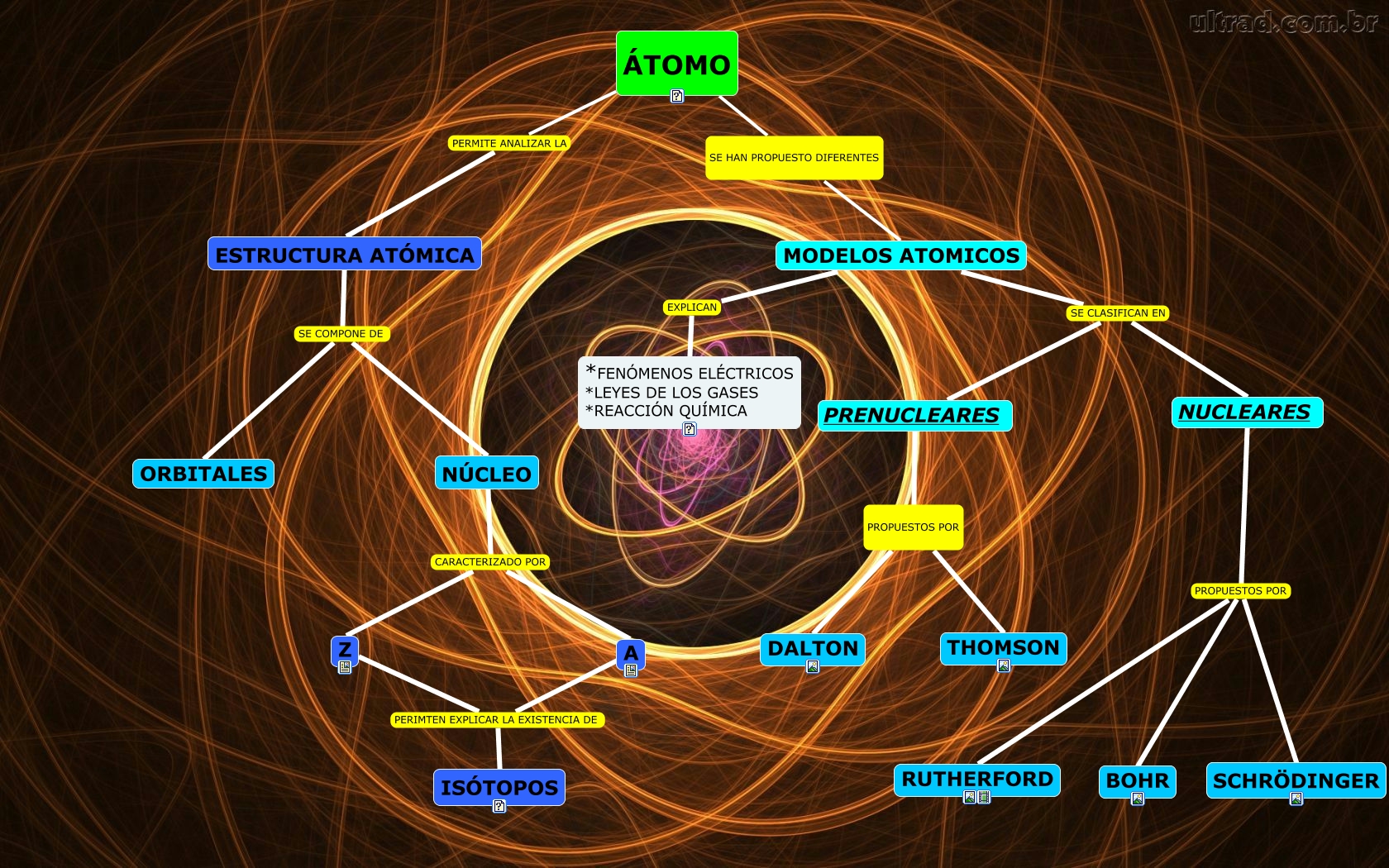
Modelo Atómico de Schrödinger
El modelo atómico de Schrödinger 1 2 (1926) es un modelo cuántico no relativista. En este modelo los electrones se contemplaban originalmente como una onda estacionaria de materia cuya amplitud decaía rápidamente al sobrepasar el radio atómico. El modelo de Bohr funcionaba para el átomo de hidrógeno. En los espectros realizados para.

Modelo atómico de Schrödinger (Modelo mecánico cuántico del átomo) YouTube
Desarrollado por Schrödinger en 1926 se basa en la teoría de un átomo cuántico. Schrödinger se apoyaría de los estudios en el modelo atómico de Sommerfeld, para postular que el comportamiento de los electrones al rededor del núcleo se debía a ondas de materia. Se calcularía como una ecuación ondulatoria que media su evolución en el.

Bienvenida Estructura Atómica Estructura Atómicas
Considerado uno de los pilares de la mecánica cuántica, el modelo de Schrödinger nos permite entender cómo se comportan los electrones en un átomo. A través de esta guía, aprenderemos las bases teóricas y matemáticas de este modelo, así como su importancia en el estudio de la estructura y propiedades de la materia.

Что находится внутри атомного ядра? NewScience.ru
Teoría atómica moderna. El trabajo de Schrodinger y Heisenberg conduce a la teoría atómica moderna , que nos muestra que existen regiones dentro de un átomo donde es probable que existan electrones. Estas regiones que contienen electrones que existen alrededor del núcleo se conocen como nubes de electrones u orbitales.

Atoms & Molecules echapter — The Biology Primer
El modelo atómico de Schrödinger se desarrolló en 1926. Se trata del modelo mecánico cuántico del átomo que partía de la ecuación de Schrödiger. Con esta ecuación se podía conocer la probabilidad de encontrar un electrón en un determinado punto de un átomo. Actualmente, no hay ningún modelo más preciso sobre la estructura del.

Nube Electrónica Quimica Quimica
El Modelo Atómico de Schrödinger: El Modelo Atómico de Schrödinger (1924) postula que: los electrones son ondas de materia que se distribuyen en el espacio según la función de ondas (Ψ): (δ2Ψ/δx2) + (δ2Ψ/δy2) + (δ2Ψ/δz2) + (8π2m/h2) (E-V)Ψ = 0. los electrones se distribuyen en orbitales que son regiones del espacio con una.

Describe The Electron Cloud Model Of The Atom Vários Modelos
¿Quién ideó el concepto del modelo de la nube de electrones? El modelo de la nube de electrones fue propuesto por Erwin Schrödinger en 1926. Esta teoría se basa en la idea de que los electrones se comportan como ondas alrededor del núcleo del átomo, en lugar de orbitar alrededor del mismo.

Erwin Schrödinger Biografía, Aportaciones, Libros, y más
Postulados del modelo atómico de Schrödinger. Los postulados del modelo atómico de Schrödinger son los siguientes: -Los electrones se comportan como ondas estacionarias que se distribuyen en el espacio según la función de onda Ψ. -Los electrones se desplazan dentro del átomo describiendo orbitales. Estas son zonas en donde la.
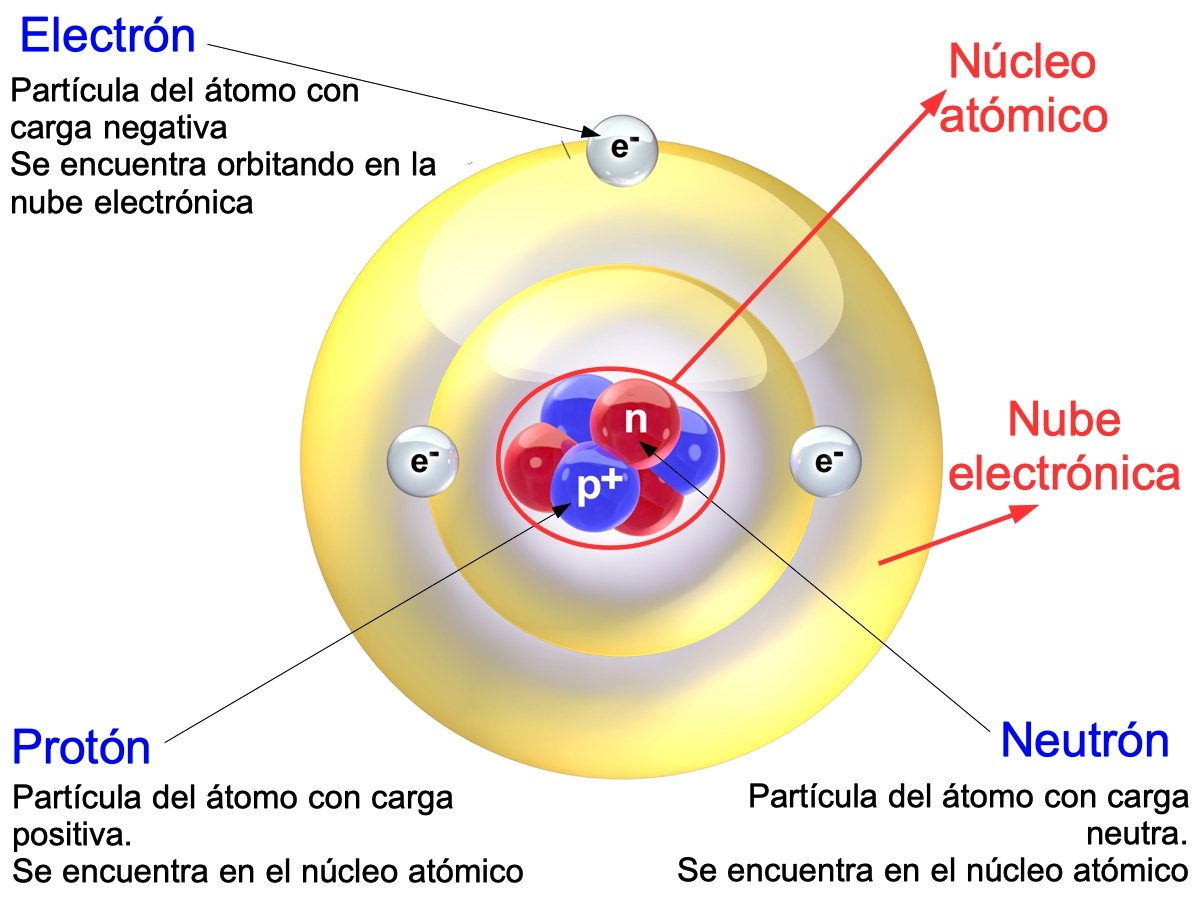
Átomo (Qué es, Partes, Estructura, Características e Historia) Enciclopedia Significados
Saltar al contenido principal.

modeloatomicoerwinschrodinger Blog de empresa logística, Recursos Humanos, comercio y finanzas
Descripción. El modelo atómico de Schrödinger describe el movimiento de electrones y ondas estacionarias. Este modelo describe que los electrones se encuentran en constante movimiento, por lo que no se encuentran en una posición estable dentro del átomo. El modelo atómico Schrödinger no predice la ubicación de cada uno de los electrones.
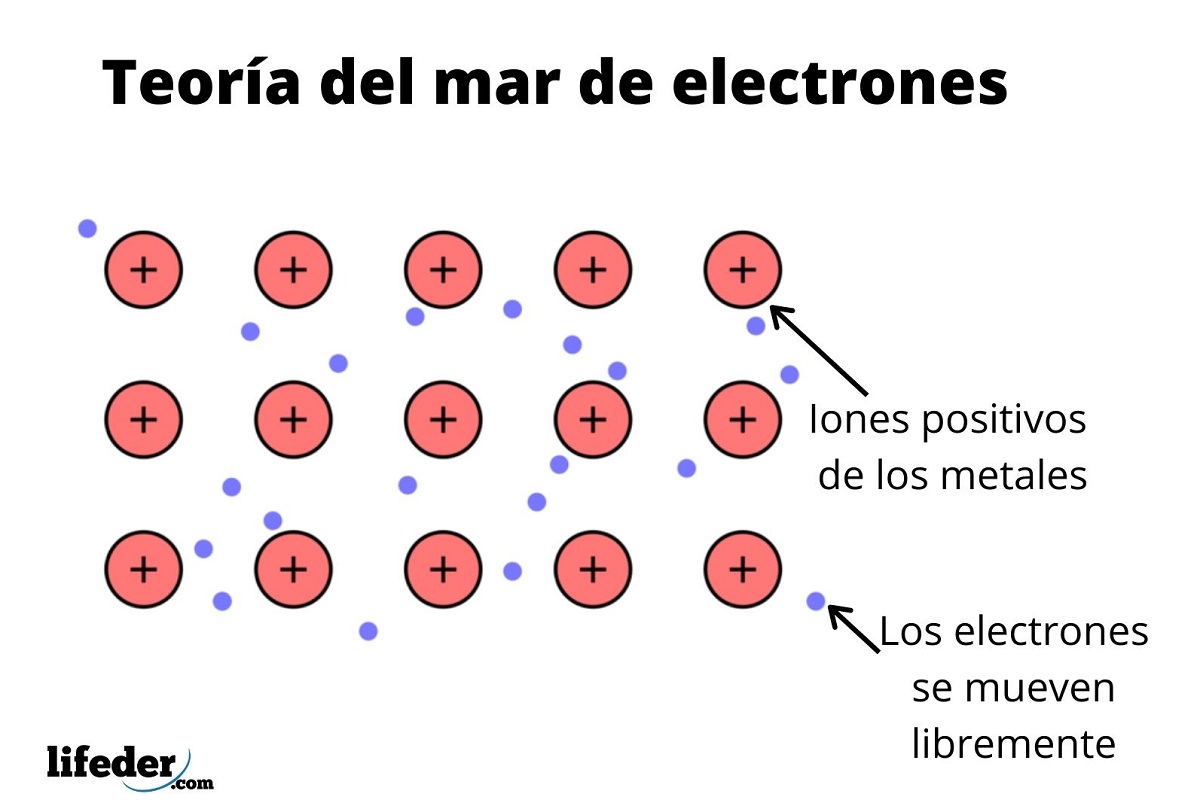
Teoría del Mar de Electrones Fundamentos y Propiedades
Notarás que la nube de electrones no tiene un color uniforme; es más oscuro en el núcleo y gradualmente se aclara a medida que te alejas.Este gradiente de color se basa en la probabilidad de electrones, la probabilidad de encontrar un electrón en una ubicación determinada.En términos generales, las posibilidades de encontrar un electrón disminuyen a medida que se aleja del núcleo.

Las 3 partes de un átomo (y sus características)
El modelo atómico de Schrödinger pretende dilucidar el movimiento del electrón y su distribución en términos de probabilidad, pero no contempla asuntos como la estabilidad del átomo o sus partes. Siguiendo la ecuación de Schrödinger se obtienen valores discretos de energía si el electrón se desplaza en un espacio delimitado.

Nube de electrones fotografías e imágenes de alta resolución Alamy
El modelo de la nube de electrones fue propuesto por Erwin Schrödinger en 1926, como parte del desarrollo de la mecánica cuántica. Este modelo describe a los electrones en un átomo no como partículas con trayectorias definidas, sino más bien como una nube de probabilidad que rodea al núcleo atómico. La posición y energía de los.

QUÍMICA ECA Enseñanza media EL ÁTOMO
Electrón: La electrón es. Una partícula cargada negativamente (libre o unida) de un átomo y la carga de un solo electrón es una unidad -ve carga. La partícula más pequeña y ligera de un átomo. Los electrones están en constante movimiento mientras circulan alrededor del núcleo.

El modelo atómico de Schrödinger explicado (postulados)👩🔬 YouTube
Puntos más importantes. Erwin Schrödinger propuso el modelo mecánico cuántico del átomo, el cual trata a los electrones como ondas de materia. , representa la probabilidad de encontrar un electrón en una región dada dentro del átomo. Un orbital atómico está definido como la región dentro de un átomo que encierra donde posiblemente.
- Vestimenta Típica De Argentina Mujer
- Receta De Sandwich De Jamon
- La Constitucion De 1857 Pdf
- Marosa Di Giorgio La Guerra De Los Huertos Pdf
- Quien Es Quien En La Serie De La Guzman
- Que Es Una Ecuacion Parametrica
- Hello My Name Is Stickers
- Formula Del Area Del Decagono
- Connected Stereo Mc Letra Traducida
- 50 Sombras De Grey Online Latino